مؤلف:
Mike Robinson
تاريخ الخلق:
7 شهر تسعة 2021
تاريخ التحديث:
11 قد 2024

المحتوى
يتوافق العدد الذري مع عدد البروتونات في نواة ذرة واحدة من عنصر. هذه القيمه لا تتغير؛ لذلك ، يمكنك استخدامه لاكتشاف خصائص أخرى للنظير ، مثل عدد النيوترونات.
خطوات
جزء 1 من 2: إيجاد العدد الذري
ابحث عن نسخة من الجدول الدوري. انقر هنا إذا لم يكن لديك واحد متاح. كل عنصر له رقمه الذري ؛ وبالتالي ، لا توجد طرق مختصرة لتعلم المحتوى. استخدم نسخة من الجدول أو حاول حفظه.
- تحتوي معظم كتب الكيمياء على الطاولة مطبوعة على الغلاف الخلفي.

ابحث عن العنصر الذي تدرسه في الجدول. تتضمن معظم الجداول الاسم الكامل للعناصر ، بالإضافة إلى رموزها (الزئبق للزئبق ، على سبيل المثال). إذا لم تتمكن من العثور على ما تبحث عنه ، فانتقل إلى الإنترنت وابحث باستخدام المصطلحات "الرمز الكيميائي" واسم العنصر.
أوجد العدد الذري للعنصر. عادة ما يكون في الزاوية العلوية اليسرى أو اليمنى من منزل العنصر ، ولكن يمكن أن يأتي أيضًا في أماكن أخرى. بالإضافة إلى ذلك ، فهي دائمًا قيمة عدد صحيح.- إذا كان الرقم يتضمن فاصلة عشرية ، فمن المحتمل أن يشير إلى الكتلة الذرية.
تأكد من المعلومات وفقًا للعناصر القريبة. الجدول الدوري منظم حسب ترتيب الأعداد الذرية. إذا كان رقم نظيرك هو "33" ، على سبيل المثال ، سيكون العنصر الموجود على اليسار هو "32" والعنصر الموجود على اليمين سيكون "34". في هذه الحالة ، لأنك تنظر إلى العدد الذري.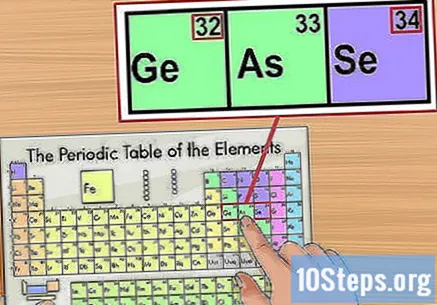
- هناك قفزة بين عنصري "56" (باريوم) و "88" (راديو). تقع النظائر التي تتوافق مع هذا النطاق في الصفين أسفل الجدول. يتم فصلهم فقط بهذا الشكل بحيث لا تكون الطاولة كبيرة جدًا.
افهم معنى العدد الذري. للعدد الذري تعريف بسيط: كمية البروتونات في ذرة العنصر. تحدد هذه الكمية من البروتونات بدورها الشحنة الكهربائية الكلية للنواة - والتي تحدد بالتالي عدد الإلكترونات التي يمكن للذرة شحنها. نظرًا لأن الإلكترونات مسؤولة عن جميع التفاعلات الكيميائية تقريبًا ، فإن العدد الذري يؤثر بشكل غير مباشر على الخصائص الفيزيائية والكيميائية للعنصر.- بمعنى آخر ، كل ذرة بها ثمانية بروتونات تقابل ذرة أكسجين. يمكن أن تحتوي ذرتان من الأكسجين على عدد مختلف من النيوترونات أو (إذا كان أحدهما أيونًا) أو إلكترونات ، ولكن سيكون لكل منهما ثمانية بروتونات دائمًا.
جزء 2 من 2: اكتشاف معلومات أكثر أهمية
حدد الوزن الذري. عادة ما يأتي تحت اسم العنصر في الجدول الدوري ويحتوي على منزلتين أو ثلاث منازل عشرية. الوزن الذري يتوافق مع متوسط كتلة ذرات العنصر ، ويمثل كيفية وجوده في الطبيعة. يقاس بوحدات الكتلة الذرية ("u" أو "u.m.a").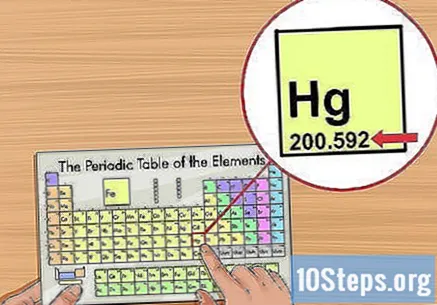
- يفضل العديد من العلماء استخدام مصطلح "الكتلة الذرية" بدلاً من الوزن.
افهم الكتلة الذرية. يشبه مفهوم الكتلة الذرية مفهوم الوزن. الفرق هو أن الوزن يشير إلى متوسط كتلة أي ذرة في العنصر ، وليس ذرة معينة. على سبيل المثال: يحتوي غرام الحديد على عدة ذرات بكتل متفاوتة ؛ الوزن يشير إلى "الكتلة النسبية". إذا درست ذرة واحدة من العنصر ، فأنت تحتاج فقط إلى معرفة كتلته المحددة.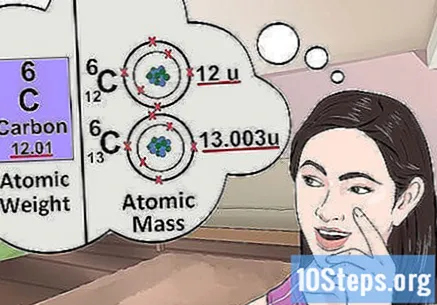
- بشكل عام ، فإن المسائل الكيميائية التي تنطوي على الذرات وحدها تحدد عدد الكتلة الذرية. تحتاج فقط إلى فهم المفهوم حتى لا تفاجأ عندما ترى قيمة مختلفة.
تقريب العدد الكتلي. يتوافق العدد الكتلي مع الكمية الإجمالية للبروتونات والنيوترونات في ذرة العنصر. حسابه ليس صعبًا: فقط خذ الكتلة الذرية المطبوعة في الجدول الدوري وقم بتقريبها إلى أقرب قيمة صحيحة.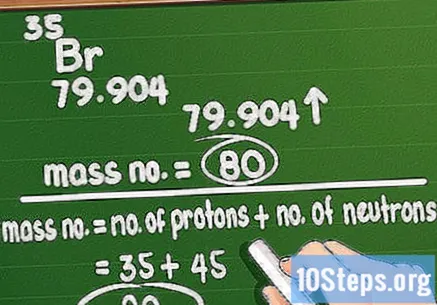
- يعمل هذا لأن كميات النيوترونات والبروتونات قريبة جدًا من 1 ميكرو أمبير ، في حين أن كمية الإلكترونات قريبة جدًا من الصفر. تتضمن الكتلة الذرية حسابات دقيقة لتحديد القيمة العشرية ، لكن البيانات الوحيدة المهمة هي الأعداد الصحيحة ، والتي تخبرك بعدد البروتونات والنيوترونات الموجودة.
- تذكر أنه إذا كنت تستخدم كتلة ذرية ، فسوف تعبث بوزن ذرة معينة في عنصر ما. عينة البروم ، على سبيل المثال ، لها كتلة ذرية من 79 أو 81.
احسب عدد النيوترونات. الآن ، أنت تعلم بالفعل أن العدد الذري يساوي عدد البروتونات وأن العدد الكتلي يساوي مجموع عدد البروتونات والنيوترونات. لتحديد كمية النيوترونات في عنصر ما ، ما عليك سوى طرح العدد الذري من إجمالي الكتلة. بعض الأمثلة:
- ذرة الهيليوم (He) لها عدد كتلي 4 وعدد ذري 2. لذلك ، 4 - 2 = 2 نيوترون.
- يبلغ متوسط عدد كتلة عينة الفضة (Ag) 108 (وفقًا للجدول الدوري) وعددها الذري 47. في المتوسط ، تحتوي كل ذرة في العينة على 108-47 = 61 نيوترون.
افهم النظائر. النظير هو شكل محدد لعنصر يحتوي على عدد من النيوترونات. إذا كانت المشكلة التي تريد حلها تأتي بشيء مثل "boron-10" أو "B" ، فذلك لأنك تتحدث عن عناصر البورون ذات العدد الكتلي 10. استخدم هذه القيمة ، وليس القيم "العادية" من البورون.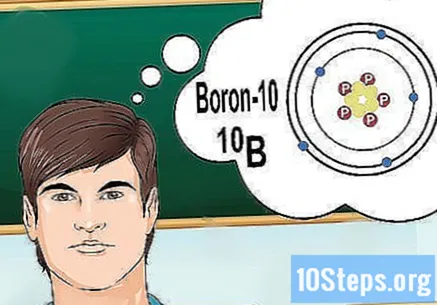
- لا يتغير العدد الذري للنظائر أبدًا. كل نظير لعنصر ما له نفس عدد البروتونات.
نصائح
- يأتي الوزن الذري لبعض العناصر الأثقل بين أقواس أو أقواس مربعة. هذا يعني أن هذا الوزن هو الكتلة الدقيقة للنظير الأكثر استقرارًا ، وليس متوسط عدد من النظائر. أخيرًا ، هذا لا يؤثر على العدد الذري للعنصر.


