المحتوى
على الرغم من أن جميع ذرات العنصر نفسه تحتوي على نفس عدد البروتونات ، إلا أن عدد النيوترونات يمكن أن يختلف. يمكن أن تساعدك معرفة عدد النيوترونات الموجودة في ذرة معينة في تحديد ما إذا كان الجسيم منتظمًا في هذا العنصر أم نظيرًا ، والذي سيكون به عدد أكبر أو أقل من النيوترونات. إن تحديد عدد النيوترونات في الذرة أمر بسيط للغاية ولا يتطلب أي تجربة. لحساب عدد النيوترونات في ذرة أو نظير عادي ، اتبع هذه التعليمات مع وجود جدول دوري في متناول اليد.
خطوات
طريقة 1 من 2: إيجاد عدد العناصر المحايدة في ذرة مشتركة
حدد موقع العنصر في الجدول الدوري. في هذا المثال ، لنلقِ نظرة على نظام التشغيل (Os) ، الموجود في الصف السادس ، من الأعلى إلى الأسفل.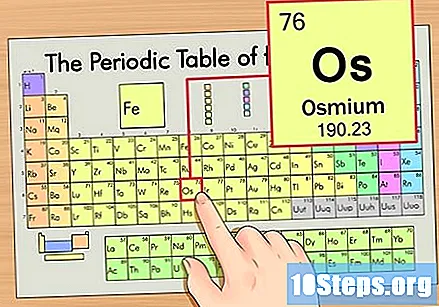
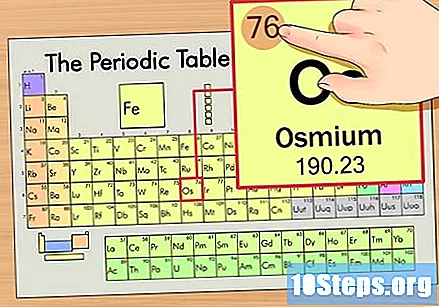
أوجد العدد الذري للعنصر. عادة ما يكون هذا هو الرقم الأكثر وضوحًا لعنصر معين وعادة ما يكون أعلى رمزه (في الجدول الذي نستخدمه ، في الواقع ، لا يوجد رقم آخر مدرج). العدد الذري هو عدد البروتونات في ذرة واحدة من هذا العنصر. عدد Os هو 76 ، مما يعني أن ذرة Osmium بها 76 بروتونًا.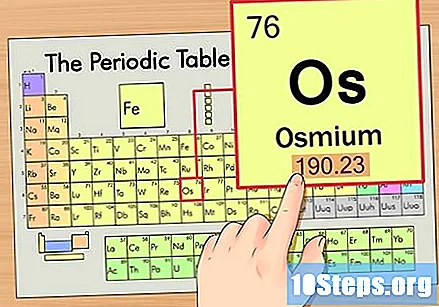
أوجد الوزن الذري للعنصر. يوجد هذا الرقم عادة أسفل الرمز الذري. لاحظ أن الجدول في هذا المثال يعتمد فقط على العدد الذري ولا يسرد الوزن الذري. ولن يكون هذا هو الحال دائما. الأوزميوم له وزن ذري 190.23.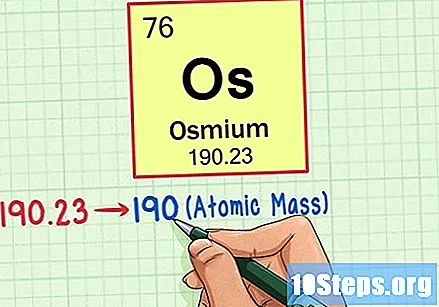
قرب الوزن الذري لأقرب عدد صحيح لإيجاد الكتلة الذرية. في مثالنا ، سيتم تقريب 190.23 إلى 190 ، مما ينتج عنه كتلة ذرية تساوي 190 للأوزميوم.- الكتلة الذرية هي متوسط نظائر العنصر. لذلك ، فهو ليس عادةً عددًا صحيحًا.
اطرح العدد الذري من الكتلة الذرية. نظرًا لأن الغالبية العظمى من كتلة الذرة موجودة في البروتونات والجسيمات المحايدة ، فإن طرح عدد البروتونات (أي العدد الذري) من الكتلة الذرية سيعطيك الرقم محسوب من النيوترونات في الذرة. يمثل الرقم بعد العلامة العشرية عمومًا كتلة صغيرة جدًا من الإلكترونات في الذرة. في مثالنا ، هذا هو: 190 (الكتلة الذرية) - 76 (عدد البروتونات) = 114 (عدد النيوترونات).
تذكر الصيغة. لمعرفة عدد النيوترونات في المستقبل ، ما عليك سوى استخدام هذه الصيغة: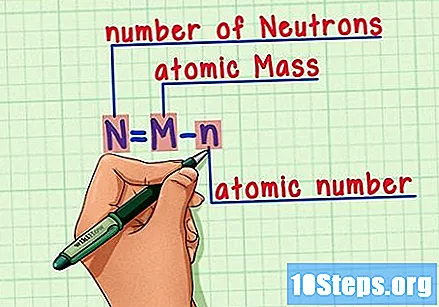
- N = م - ن.
- N = عدد نالأترونات.
- م = مالشواء الذري.
- ن = نعظم العضد الذري.
- N = م - ن.
طريقة 2 من 2: إيجاد عدد النيوترونات في نظير
حدد موقع العنصر في الجدول الدوري. على سبيل المثال ، دعنا نستخدم نظير الكربون 14. نظرًا لأن الشكل غير النظيري للكربون 14 هو ببساطة كربون (C) ، ابحث عن هذا العنصر في الجدول الدوري (في الصف الثاني).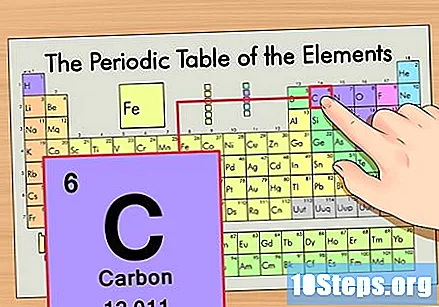
أوجد العدد الذري للعنصر. عادة ما يكون هذا هو الرقم الأكثر وضوحًا لعنصر معين وعادة ما يكون أعلى رمزه (في الجدول الذي نستخدمه ، في الواقع ، لا يوجد رقم آخر مدرج). العدد الذري هو عدد البروتونات في ذرة واحدة من هذا العنصر. C هو رقم 6 ، مما يعني أن ذرة الكربون تحتوي على 6 بروتونات.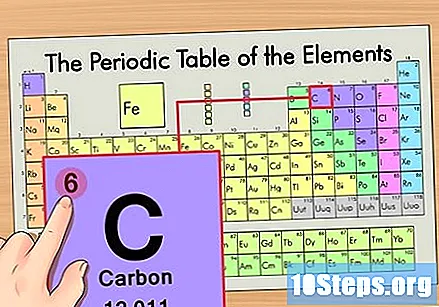
أوجد الكتلة الذرية. هذا سهل للغاية مع النظائر ، حيث سميت على اسم كتلتها الذرية. كتلة ذرية للكربون 14 تساوي 14. بمجرد إيجاد الكتلة الذرية للنظير ، فإن عملية إيجاد عدد النيوترونات هي نفسها المستخدمة مع الذرات العادية.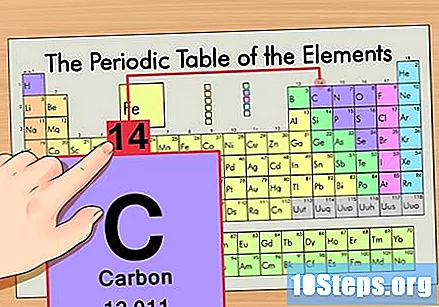
اطرح العدد الذري من الكتلة الذرية. نظرًا لأن الغالبية العظمى من كتلة الذرة موجودة في البروتونات والجسيمات المحايدة ، فإن طرح عدد البروتونات (أي العدد الذري) من الكتلة الذرية سيعطيك الرقم محسوب من النيوترونات في الذرة. يمثل الرقم بعد العلامة العشرية عمومًا كتلة صغيرة جدًا من الإلكترونات في الذرة. في مثالنا ، هذا هو: 14 (الكتلة الذرية) - 6 (عدد البروتونات) = 8 (عدد النيوترونات).
تذكر الصيغة. لمعرفة عدد النيوترونات في المستقبل ، ما عليك سوى استخدام هذه الصيغة: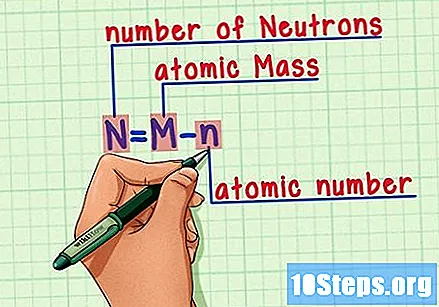
- N = م - ن.
- N = عدد نالأترونات.
- م = مالشواء الذري.
- ن = نعظم العضد الذري.
- N = م - ن.
نصائح
- الأوزميوم ، معدن صلب في درجة حرارة الغرفة ، اشتق اسمه من الكلمة اليونانية التي تعني "رائحة" ، "أوسمي".
- تشكل البروتونات والنيوترونات الوزن الكلي للعناصر تقريبًا ، بينما تمثل الإلكترونات والجسيمات المتنوعة الأخرى كتلة ضئيلة (تقترب من الصفر). نظرًا لأن البروتون له نفس وزن البروتونات تقريبًا ويمثل العدد الذري عدد البروتونات ، يمكننا ببساطة طرح عدد البروتونات من الكتلة الكلية.
- إذا لم تكن متأكدًا من الرقم الموجود في الجدول الدوري ، تذكر فقط أنه يتم تكوينه عادةً حول العدد الذري (أي عدد البروتونات) ، والذي يبدأ بـ 1 (الهيدروجين) ويصعد بمقدار وحدة واحدة لكل من اليسار إلى اليمين ، تنتهي بـ 118 (Ununóctio). هذا لأن عدد البروتونات في الذرة يحدد ماهية تلك الذرة ، مما يسهل تنظيم الخاصية الأولية (على سبيل المثال ، ستكون الذرة التي تحتوي على بروتونين دائمًا هيليوم ، تمامًا مثل ذرة أخرى بها 79 بروتونًا ستكون دائمًا ذهبية).